Onco-Digestif
Carcinome épidermoîde du canal anal traité par chimioradiothérapie : l'ADN tumoral circulant comme marqueur de réponse
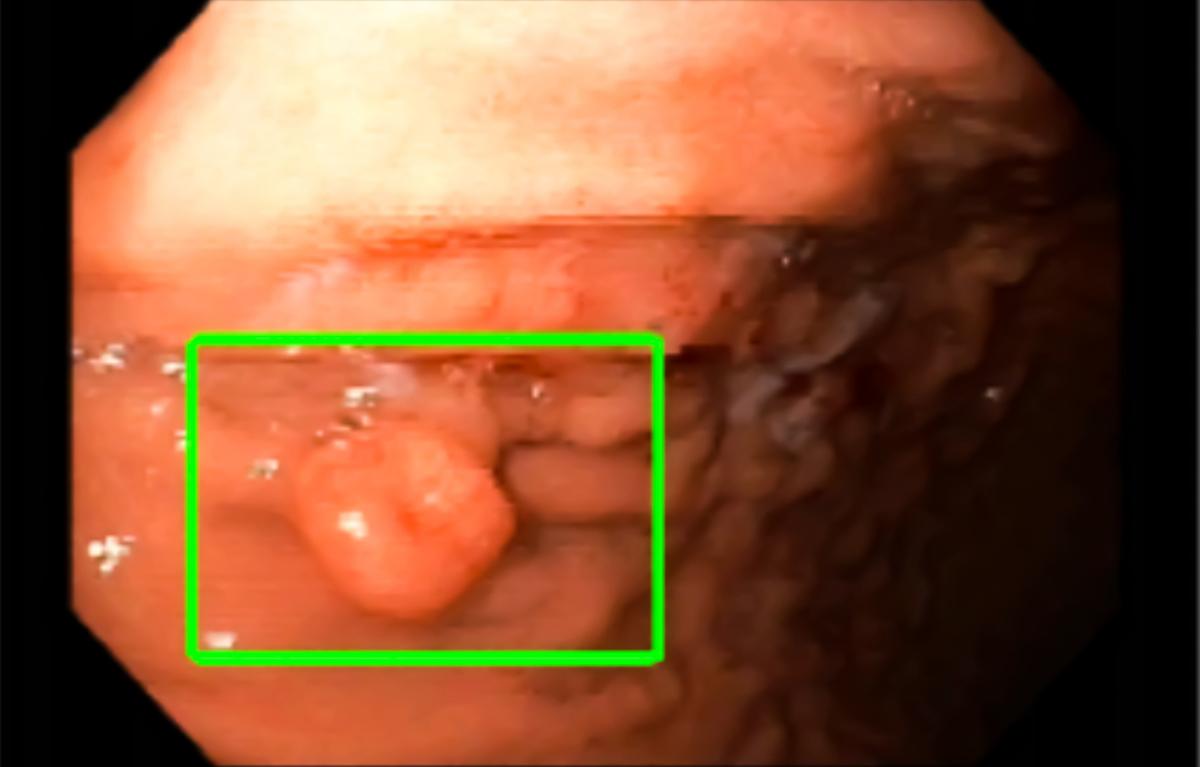
L’incidence des carcinomes épidermoïdes du canal anal est en augmentation, liée à la fréquence des infections par HPV. Le plus souvent diagnostiqués à un stade localisé, leur traitement repose sur la chimioradiothérapie. Malgré sa bonne efficacité, environ 20 % des patients vont présenter une rechute [1]. Dans ce contexte, un biomarqueur permettant de détecter précocement une rechute pourrait être utile.

- Rasi Bhadramani/iStock
L'ADN tumoral circulant (ctDNA) s'est révélé un outil prometteur pour évaluer l'efficacité du traitement et prédire le pronostic dans plusieurs pathologies cancéreuses telles que le cancer du côlon ou le cancer du sein. Cependant, il y a peu de données pour les cancers du canal anal. Dans cette étude de suivi longitudinale ont été inclus 88 patients traités pour un carcinome épidermoïde du canal anal par chimioradiothérapie [Bercz A 3518]. La présence de ctDNA était recherchée par un prélèvement sanguin avant le traitement, à mi-traitement et après le traitement puis pendant la surveillance tous les trois mois. La présence ou l’absence de ctDNA a été corrélée à l’échec locorégional (LRF) et à la survie sans progression (PFS).
La disparition du ctDNA après traitement est corrélée à la survie
Les patients présentaient majoritairement des tumeurs de stade II et III et 87 % étaient HPV+. Le suivi médian était de 18 mois. Au total, 647 prélèvements ont été analysés avec le test Signatera (Natera, Inc.). La présence de ctDNA était retrouvée chez 79 % des patients avant le traitement. Ces résultats variaient en fonction du stade tumoral (30% pour les stades I, 90 % pour les stades III). Après le traitement, 92 % n’avaient plus de ctDNA. Pendant le suivi, sept patients ont présenté une LRF et cinq ont présenté des métastases à distance. Aucun des patients dont le ctDNA était négatif à mi-traitement n’ont présenté de LRF. À l'inverse, 26 % des patients présentant une positivité du ctDNA à mi-traitement et 61 % des patients présentant une positivité du ctDNA après le traitement ont présenté une LRF. Alors que la présence de ctDNA avant traitement n’avait pas de valeur pronostique, la présence de ctDNA post-traitement était significativement corrélée avec un taux de survie globale à 1 an diminué (96 % versus 63 %, p = 0,002). La présence de ctDNA post-traitement était également significativement corrélée avec la PFS, ainsi que la présence de ctDNA à mi-traitement. Parmi les patients qui ont présenté une négativité du ctDNA post-traitement mais pour lesquels il est ensuite réapparu pendant la surveillance, tous ont développé une rechute tumorale. Dans tous les cas, la rechute moléculaire a précédé la découverte clinique ou radiographique.
Un recul plus long ainsi qu’une validation dans de plus larges cohortes prospectives est nécessaire avant de pouvoir conclure sur l’utilité clinique de ce test dont les résultats sont prometteurs.